Este post mostra o conceito de pH e sua influência no ciclo do nitrogênio. É uma continuação do post anterior sobre Meio Ambiente.
Para saber o que é o ciclo do nitrogênio, clique no botão a seguir.
Ciclo do nitrogênioClique aqui
O que é o pH?
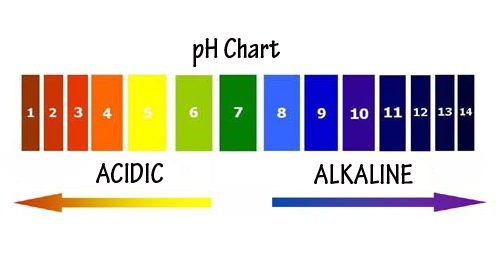
É a abreviatura de potencial hidrogeniônico e uma medida de escala logarítmica, que indica o grau de acidez ou alcalinidade em uma solução. Quanto maior a quantidade de íons de hidrogênio (H^{+}) dissolvidos em solução aquosa, mais ácida é a substância.
Cálculo
O pH é o logaritmo negativo da concentração de H^{+} em mol/l na base 10.
pH=-log[H^{+}]
[H^{+}]=10^{-pH}
Esta equação mostra que cada número possui 10 vezes mais concentração de H^{+} em meio aquoso do que o número maior. Por exemplo, uma substância com pH igual a 5 é 10 vezes mais ácido do que uma solução com pH de 6.
A influência do pH no ciclo do nitrogênio
As plantas terrestres usam a amônia para sintetizar aminoácidos. No meio aquático, a amônia (NH_{3}) é tóxica para os peixes. Esta molécula pode atravessar as guelras do peixe. Quando estiver dentro da guelra, pode se converter em íon amônio (NH_{4}^{+}), esta conversão causa dano às células.

Além disso, o excesso de NH_{3} prejudica o esqueleto dos corais, tornando-os menos denso. No entanto, o NH_{4}^{+} não é tóxico para os peixes, pois não consegue entrar nas guelras.
Princípio de Le Chatelier no ciclo do nitrogênio
A amônia forma um equilíbrio com o íon amônio, mostrado pela seguinte reação química reversível.
NH_{3}+H_{2}O\rightleftharpoons NH_{4}^{+}+OH^{-}
Um sistema químico está em equilíbrio quando a velocidade das reações nos dois lados da equação reversível são iguais e quando a concentração das substâncias envolvidas são constantes. O princípio de Le Chatelier afirma que, quando o equilíbrio de um sistema químico é perturbado por um fator externo, este sistema se reajusta para ficar em um novo equilíbrio. No sistema químico acima, que é parte do ciclo do nitrogênio, quanto menor o pH da água, maior a produção de NH_{4}^{+}.




Thank you for your sharing. I am worried that I lack creative ideas. It is your article that makes me full of hope. Thank you. But, I have a question, can you help me?